Bikin Vaksin Jangan Grusa-grusu, Akibatnya Bisa Fatal!
Jakarta, CNBC Indonesia - Mengembangkan dan membuat vaksin yang efektif untuk menangkal patogen bukanlah pekerjaan mudah dan tak bisa tergesa-gesa. Pasalnya jika vaksin tersebut terlalu diburu-buru tanpa melihat aspek keamanan dan efektivitasnya, dampak yang ditimbulkan bisa sangat membahayakan.
Pertimbangan inilah yang membuat kandidat vaksin yang dikembangkan Rusia bernama 'Sputnik V' itu mengundang kontroversi. Pro-kontra di kalangan publik tak terlepas dari klaim Putin bahwa Rusia menjadi negara pertama yang berhasil mengembangkan vaksin untuk virus corona.
Kandidat vaksin Rusia tersebut dikembangkan oleh Gamaleya Research Institute. Mengingat kandidat tersebut baru saja masuk tahap uji klinis fase I/II pada 17 Juni, pernyataan Putin pun menimbulkan keraguan di kalangan banyak pihak terutama para ilmuwan.
Bahkan ketika 'Sputnik V' belum merilis hasil resmi uji klinis tahap awalnya dan juga belum masuk fase III, Presiden Negeri Beruang Merah itu sudah mengatakan ada 20 negara yang sudah mengantre membeli vaksin tersebut.
Putin bahkan tak ragu mengatakan bahwa vaksin tersebut telah disuntikkan ke putrinya dan kini anaknya tersebut dalam kondisi sehat meski sempat dilaporkan mengalami demam hingga 38 derajat celcius pasca injeksi.
"Anda tidak bisa menggunakan vaksin atau obat tanpa melalui semua fase uji klinis tersebut" kata Dr. Jarbas Barbosa, Asisten Direktur WHO untuk Pan American Health Organization.
"Saat ini WHO sedang mengontak regulator kesehatan Rusia untuk mendapatkan informasi terkait vaksin ini dan setelah melakukan analisa dari informasi yang didapat, barulah WHO bisa memberikan rekomendasi."
Pada kondisi normal saja tanpa pandemi, pengembangan vaksin membutuhkan waktu 5-8 tahun. Bahkan sampai ada yang 12 tahun. Sejarah mencatat pengembangan vaksin paling cepat adalah untuk penyakit gondok yang menelan waktu empat tahun sebelum disetujui pada 1967.
Namun pada dasarnya agar vaksin dapat mencapai ke pasaran atau publik setidaknya ada enam tahapan yang harus dilalui.
Pertama jelas riset dan pengembangan, kemudian persiapan pre-klinis dengan mengujinya pada hewan model, baru uji klinis yang jumlahnya ada tiga tahap, barulah disetujui dan diproduksi skala masif hingga didistribusikan.
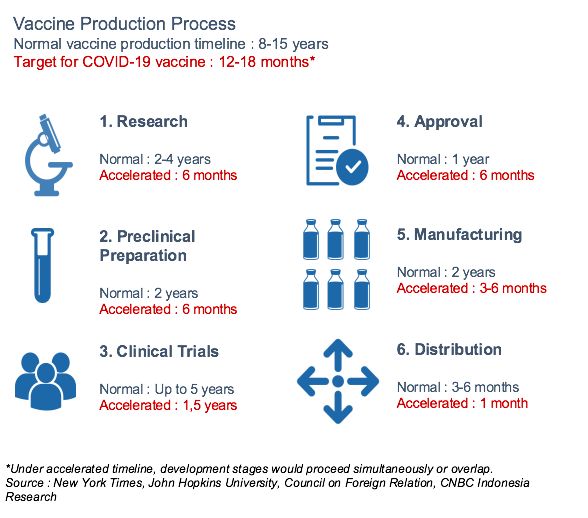 |
Melihat urgensi yang terjadi sekarang, timeline pengembangan vaksin untuk virus corona dipercepat menjadi 12-18 bulan saja. Meski ilmu pengetahuan dan teknologi sudah sangat berkembang pesat, waktu pengembangan yang dipadatkan ini pun masih mendapat pandangan skeptis dari banyak ilmuwan.
Hal yang harus ditekankan bukanlah menjadi penemu pertama dari vaksin, tetapi yang lebih penting adalah untuk menyediakan vaksin yang jelas aman serta efektif untuk populasi dunia yang saat ini tengah terancam pandemi global.
Aspek safety & efficacy adalah poin utama pengembangan vaksin dan tidak bisa dikesampingkan. Kita juga harus berkaca pada sejarah bahwa vaksin meski sudah mendapat persetujuan dari otoritas pengawas kesehatan ada juga yang gagal dan menyebabkan vaksin tersebut harus ditarik dari peredaran.
Mengacu pada data Center for Disease Control & Prevention (CDC) AS, pada 1955-2013 ada 10 kejadian yang menyangkut aspek keamanan dari vaksin di mana 6 vaksin penangkal dari berbagai penyakit yang sudah beredar memicu terjadinya insiden yang tak diinginkan bahkan sampai ada yang ditarik dari peredaran.
Berikut ini adalah insiden-insiden yang pernah terjadi terkait vaksin yang sudah beredar di AS menurut CDC :
Insiden Cutter - (1955)
Pada tahun 1955, beberapa batch vaksin polio yang diberikan kepada masyarakat mengandung virus polio hidup, meskipun telah lolos uji keamanan yang dipersyaratkan. Lebih dari 250 kasus polio dikaitkan dengan vaksin yang diproduksi oleh satu perusahaan: Laboratorium Cutter. Kasus yang kemudian dikenal dengan Insiden Cutter ini mengakibatkan banyak kasus kelumpuhan. Vaksin ditarik kembali segera setelah kasus polio terdeteksi.
Simian Virus 40 (SV40) - (1955-1963)
Pada periode 1955-1963, diperkirakan 10-30% dari vaksin polio yang beredar di AS terkontaminasi dengan virus simian 40 (SV40). Virus tersebut berasal dari kultur sel yang digunakan untuk membuat vaksin polio saat itu.
Sebagian besar kontaminasi terdapat pada vaksin polio yang dilemahkan (IPV), tetapi juga ditemukan pada vaksin polio oral (OPV). Setelah kontaminasi ditemukan, pemerintah AS menetapkan persyaratan pengujian untuk memverifikasi bahwa semua banyak vaksin polio baru bebas dari SV40.
Vaksin Flu Babi dan Guillain-Barre Syndrome - (1976)
Pada tahun 1976 ada peningkatan kecil risiko gangguan neurologis serius yang disebut Sindrom Guillain-Barré (GBS) setelah vaksinasi dengan vaksin flu babi.Peningkatan risiko sekitar 1 kasus tambahan GBS untuk setiap 100.000 orang yang mendapat vaksin flu babi.
Ketika lebih dari 40 juta orang divaksinasi flu babi, pejabat kesehatan federal memutuskan bahwa kemungkinan ada keterkaitan antara GBS dengan vaksin, sehingga membuat program imunisasi tersebut dihentikan.
Vaksin Rotavirus dan Intusepsi - (1998-1999)
Pada tahun 1998, FDA menyetujui vaksin RotaShield, vaksin pertama untuk mencegah gastroenteritis yang disebabkan oleh rotavirus. Tak lama setelah mendapat izin, beberapa bayi mengalami intususepsi (jenis obstruksi usus yang jarang terjadi yang terjadi saat usus terlipat dengan sendirinya) setelah divaksinasi.
Pada awalnya, tidak jelas apakah vaksin atau faktor lain yang menyebabkan gangguan usus. CDC segera merekomendasikan agar penggunaan vaksin dihentikan dan segera memulai dua penyelidikan darurat untuk mengetahui apakah menerima vaksin RotaShield menyebabkan beberapa kasus intususepsi.
Penarikan Vaksin Haemophilus influenza type b - (2007)
Pada tahun 2007, Merck & Company, Inc. secara sukarela menarik kembali 1,2 juta dosis vaksin Haemophilus influenzae tipe b (Hib) karena kekhawatiran tentang potensi kontaminasi dengan bakteri yang disebut B. cereus.
Penarikan kembali adalah tindakan pencegahan, dan setelah peninjauan yang cermat, untungnya tidak ada bukti infeksi B. cereus yang ditemukan pada penerima vaksin Hib yang ditarik kembali.
Penarikan Vaksin HPV - (2013)
Pada tahun 2013, Merck & Company, Inc. menarik kembali satu batch dari Gardasil, vaksin human papillomavirus (HPV). Penarikan kembali adalah tindakan pencegahan setelah terjadi kesalahan dalam proses pembuatan.
Perusahaan khawatir sejumlah kecil botol mungkin berisi partikel kaca karena pecah. Tidak ada masalah kesehatan yang dilaporkan terkait dengan penarikan ini selain efek samping yang diketahui yang dapat diakibatkan dari vaksinasi apa pun, seperti kemerahan pada lengan dan nyeri di tempat suntikan diberikan.
Dari insiden-insiden di atas tentunya kita harus mengambil pelajaran bahwa vaksin bukanlah 'barang' yang mudah untuk di buat. Bahkan setelah mendapatkan lisensi pun bisa saja terjadi insiden sehingga harus dimonitor dengan ketat.
Sikap optimisme memang sah-sah saja dan harus. Namun jangan sampai menjadi overconfidence atau bahkan grusa-grusu yang jelas sangat membahayakan keselamatan umat manusia.
TIM RISET CNBC INDONESIA
(twg/twg) Add as a preferred
as a preferred
source on Google [Gambas:Video CNBC]